El empleo de placebos en los ensayos clínicos
25 de mayo de 2021
|
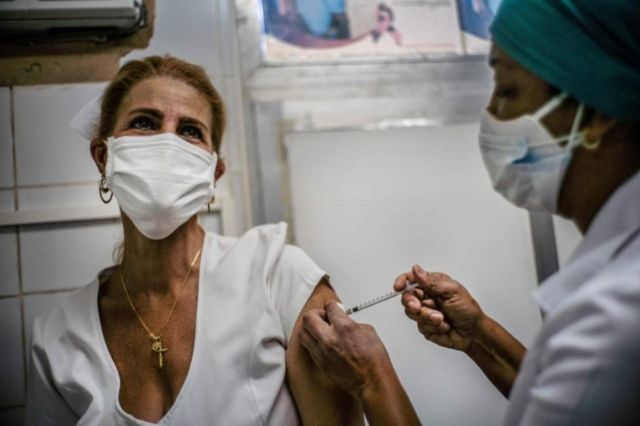
Un tema relacionado con los ensayos clínicos de los candidatos vacunales contra la Covid-19 que se están desarrollando en el presente, que ha acaparado la atención de la población, es sin lugar dudas el relativo al uso de placebos.
Por definición, se denomina placebo a una intervención diseñada para simular una terapia médica, que no tiene efectos específicos para la condición en que está siendo aplicada.
El diccionario de la Real Academia Española, por su parte, plantea que el placebo es una “sustancia que, careciendo por sí misma de acción terapéutica, produce algún efecto curativo en el enfermo si este la recibe convencido de que esa sustancia posee realmente tal acción”.
De acuerdo a su naturaleza, los placebos pueden ser puros o inactivos e impuros o activos. Los puros o inactivos son sustancias inertes que no tienen acción farmacológica en el paciente, mientras que los impuros o activos son sustancias con efectos farmacológicos potenciales, pero sin actividad específica para la condición tratada.
En el ámbito de la investigación clínica, el uso de placebo está restringido a probar la eficacia de un nuevo fármaco o procedimiento terapéutico. En ese sentido, se plantea que el ensayo clínico aleatorizado controlado con placebo a doble ciego, es considerado el mejor diseño para la evaluación de nuevos tratamientos según los principios científicos vigentes. Mediante este, un grupo de pacientes reciben tratamiento con la droga en evaluación y el otro solo recibe el placebo
De acuerdo a los beneficios que se generan, los estudios controlados con placebo resultan ventajosos por su capacidad para determinar la eficacia y seguridad de un nuevo tratamiento. Son eficientes, pues requieren menos pacientes y proporcionan un resultado más rápido. También, minimizan el efecto de las expectativas del sujeto en estudio y de los investigadores.
La desventaja del uso de placebo como control en un ensayo clínico, estriba en el hecho de que dicho grupo de participantes no recibirá un tratamiento farmacológicamente activo. Esto no genera problemas cuando no existe otro tratamiento disponible, pero en caso de existir un tratamiento estándar de eficacia probada, el uso de placebo desafiaría la obligación terapéutica de brindar el mejor tratamiento existente a estos pacientes y por ello no sería considerado ético.
Esta es la razón por la que los aspectos éticos relacionados con la utilización de placebo como control son objeto de un tratamiento muy riguroso dentro de la propia concepción de cualquier ensayo clínico, sobre la base de los principios que establece la Declaración de Helsinki.
Dicho documento es el principal código ético de comportamiento en la investigación con seres humanos en el ámbito internacional y en su contenido, aparecen contemplados los casos en que se considera éticamente aceptable la utilización de placebos en la investigación clínica.
En el particular de los ensayos clínicos de las vacunas, los placebos han sido una pieza esencial desde hace décadas, pero en su uso es fundamental que ni los voluntarios ni el personal que participa en el ensayo sepan a quién se asigna aleatoriamente cada producto, ya que con este “cegamiento” se elimina la posibilidad de que las personas se comporten de manera diferente según el agente que reciban, lo cual podría sesgar notablemente los resultados.
Galería de Imágenes
Comentarios